Квантовый химик из МГУ Татьяна Домрачева в составе большой французской коллаборации учёных вместе с коллегами из Германии и США расшифровала механизм работы одного из редких и важных природных соединений – фотофермента FAP. Фермент занимается тем, что превращает жирные кислоты в предельные углеводороды. Результат работы опубликован в журнале Science 8 апреля 2021 года.
Природные фотоферменты – исключительные по своей важности молекулы. Хотя в живой природе редко встречается применение солнечного света для катализа химических реакций, все известные фотоферменты играют ключевую роль в развитии живых организмов в таких процессах как фотосинтез и сохранение генетической информации. Учёные знают только о трёх природных ферментах, работающих как фотокатализаторы. Первый – это ДНК-фотолиаза, которая участвует в ремонте ДНК, поврежденной ультрафиолетом. Второй фермент – LPOR – отвечает за последнюю стадию синтеза молекулы хлорофилла. Прежде чем говорить о третьем, стоит осознать то, что только за исследования перечисленных веществ и механизмов как минимум пять раз вручались Нобелевские премии по химии – в 1915, 1961, 1980, 1988, и 2015 годах.
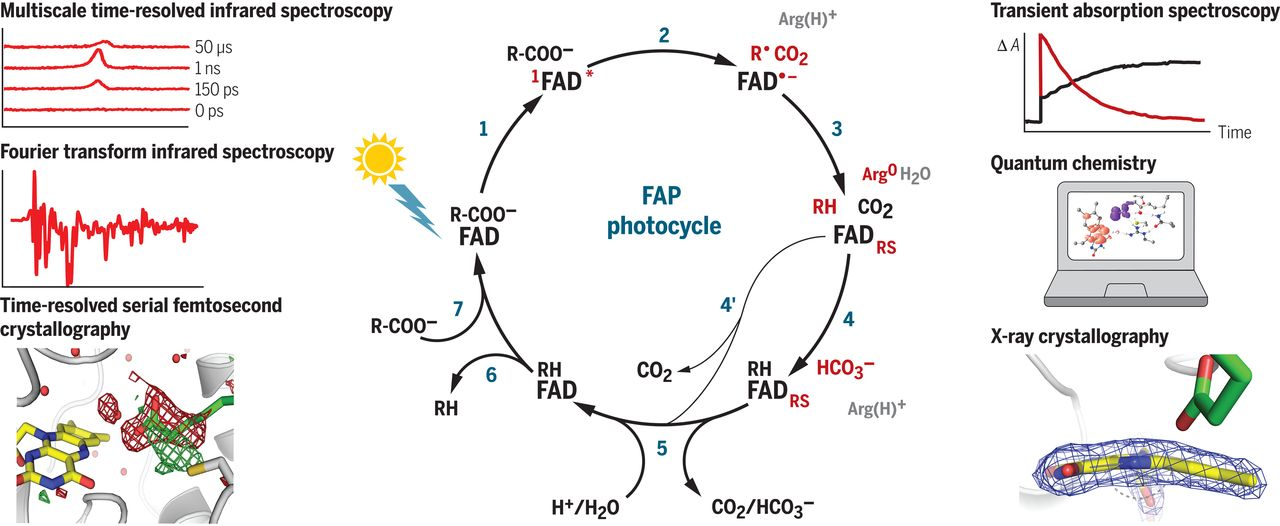
Третий фермент называется FAP, что расшифровывается как фотодекарбоксилаза жирных кислот. Его открыли французские ученые в 2016 году. FAP встречается, в частности, в одноклеточных водорослях. И пока ученые в деталях не знали, как именно с его помощью жирные кислоты в одну стадию превращаются в предельные углеводороды. «Знать механизм реакции, которую катализирует FAP, важно не только с точки зрения фундаментальной науки, но и для потенциального использования фотокатализа в биотехнологии, – рассказала с.н.с. кафедры физической химии химического факультета МГУ к.х.н. Татьяна Домрачева. – Во-первых, жирные кислоты присутствуют во всех живых организмах. И используя данную реакцию, мы получаем возобновляемый источник самых энергетически насыщенных углеводородов – предельных. Причем, речь идёт о реакции одностадийной, что критически важно для промышленных процессов. Реакция проходит в водной среде, что избавляет нас от органических растворителей и полностью соответствует принципам “Зелёной химии”. Во-вторых, это ещё один важный шаг к пониманию механизмов так называемого углеводородного цикла, который описывает механизмы превращения углеводородных запасов в мировом океане. В-третьих, мы столкнулись с тем, что, возможно, сложные органические молекулы могут функционировать при помощи нескольких параллельных механизмов. Это ставит под сомнение некоторые представления о биохимических реакциях, существующие в научной среде, и требует отдельного осмысления».
Чтобы детально понять механизм работы FAP, группа ученых из 12 ведущих французских, германских, американских университетов и МГУ работала больше трёх лет, рассказывает Татьяна Домрачева: «Коллеги изучали систему практически всеми возможными методами, кроме, пожалуй, спиновых исследований. Моя же задача как квантового химика состояла в том, чтобы на основе получаемых данных, используя методы компьютерной химии, определить наиболее вероятный механизм реакции».
В результате совместной работы был собран обширный материал, который авторы решили не делить на отдельные статьи, и опубликовать целиком. «Нам кажется, что подобный подход критически важен в современных условиях, когда опубликовать статью стало намного проще. При дроблении материала появляется слишком много предварительных версий и интерпретаций. Наш подход заключался в том, чтобы собрать в одну большую команду ведущих специалистов, изучающих функционирование биологических молекул различными физико-химическими методами, и максимально полно исследовать систему в рамках тесного взаимодействия».
Сейчас французские коллеги работают над созданием на основе FAP биотехнологической системы для одностадийного синтеза длинноцепочечных углеводородов, так как современные технологии вполне позволяют вывести работу фермента на промышленный уровень. К тому же, понимая механизм работы FAP, можно модифицировать фермент, улучшив его свойства и сделав более удобным в применении.